
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Gilteritinibfumarat
2023-12-02
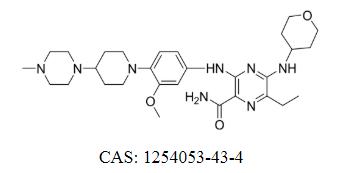
Gilteritinibfumarat Cas: 1254053-43-4
1. Hintergrund
Gezielte Medikamente gegen Gillette-Krankheit (Gilteritinib) für Patienten mit akuter myeloischer Leukämie leben länger und besser. Die kürzlich im New England Journal of Medicine veröffentlichten Ergebnisse einer großen klinischen Studie zeigen, dass im Vergleich zur Chemotherapie der Einsatz gezielter Medikamente gegen Gillette-Krankheit (Gilteritinib, Handelsname Die Behandlung mit Xospata kann die Überlebensrate von Patienten mit akuter myeloischer Leukämie (AML) etwas verbessern.
Die Ergebnisse der neuen Studie sind ermutigend. Bei den 371 in die Studie aufgenommenen Patienten handelte es sich um AML-Patienten mit einer spezifischen Mutation des FLT3-Gens, die zuvor behandelt worden waren, aber später einen Rückfall erlitten oder nicht auf die Behandlung ansprachen (rezidivierend/refraktär). Sie wurden nach dem Zufallsprinzip entweder einer Gilteritinib-Behandlung oder einer Standard-Chemotherapie zugeteilt.
Die Ergebnisse zeigten, dass Patienten, die wegen der Einnahme von Gillett und Gilteritinib behandelt wurden, nicht nur länger leben als Patienten, die sich einer Chemotherapie unterziehen (die mittlere Gesamtüberlebenszeit betrug 9,3 bis 5,6 Monate), sondern auch eine höhere Wahrscheinlichkeit haben, eine vollständige Remission zu erreichen und die Anzahl der weißen Blutkörperchen wieder auf ein normales Niveau zu bringen ganz oder teilweise (mit Gilteritinib behandelte Patienten (34 %), 15 %) bei Patienten, die sich einer Chemotherapie unterziehen.
2. Präsentation
Das von Astellas entwickelte Gilteritinib-Fumarat wurde am 21. September 2018 von der japanischen Pharmaceutical Medical Devices And Devices Integrated Agency (PMDA) zugelassen, anschließend am 28. November 2018 von der US-amerikanischen Food and Drug Administration (FDA) und von der European Drug Administration (EMA) am 24. Oktober 2019 unter dem Handelsnamen Xospata® zugelassen. Gilteritinib hat von der FDA den Fast-Track- und Orphan-Drug-Status erhalten.
Gilteritinibfumarat ist ein FLT3/AXL-Inhibitor und Xospata® ist für die Behandlung von wiederkehrender oder refraktärer akuter myeloischer Leukämie mit positiver FLT3-Mutation zugelassen.
Xospata® ist eine Tablette zum Einnehmen, die 40 mg Gilteritinib enthält. Die empfohlene Dosis beträgt 120 mg einmal täglich. Erhöhen oder verringern Sie die Dosis entsprechend dem Zustand des Patienten, sollte jedoch 200 mg pro Tag nicht überschreiten.
3. Zielpunkt
AXL; FLT3
4. Wirkmechanismus
AXL-Rezeptor-Inhibitoren; FLT3-Inhibitoren
5. Hinweise
Akute myeloische Leukämie
6. Entwicklungsstadium
Zur Vermarktung freigegeben am 21. September 2018
7. F&E-Unternehmen
Astellas
8. Syntheseweg
8.1. Die ursprüngliche Route
8.2. Unsere Route (optimiert) – Bessere Stabilität und höherer Ertrag
8.3. Ros von KSM [CAS 2043020-03-5]
8.4. Kurzer Herstellungsprozess [CAS 2043020-03-5]
Schritt 1:
Zu einer NaOH-Suspension wurde Ethyl-3-oxopentanoat in einer Portion gegeben und dann wurde die Reaktionsmischung bei Raumtemperatur gerührt. Eine Lösung von NaNO2 in Wasser wurde zugegeben und dann wurde H2SO4 tropfenweise zugegeben. Eine NaOH-Lösung wurde tropfenweise zugegeben und die resultierende Mischung mit MTBE extrahiert. Die vereinigten organischen Schichten wurden mit Kochsalzlösung gewaschen, über Na2SO4 getrocknet, filtriert und konzentriert, um das Produkt (E)-2-Oxobutanoxim zu ergeben.
Schritt 2:
Eine Suspension von (E)-2-Oxobutanaloxim und Aminomalononitril (p-Toluolsulfonsäure in IPA) wurde bei Raumtemperatur unter Argon gerührt. Nach Überprüfung durch DC wurde die Reaktionsmischung filtriert, der Kuchen wurde mit IPA und Wasser gewaschen und getrocknet, um 2-Amino-3-cyano-5-ethylpyrazin-1-oxid zu ergeben.
Schritt 3:
Zu einer Suspension von 2-Amino-3-cyano-5-ethylpyrazin-1-oxid in wasserfreiem DMF wurde POCl3 bei 0 °C gegeben. Die resultierende Mischung wurde bei 80 °C gerührt. Nach Überprüfung durch DC wurde die Reaktionsmischung langsam in Eis/Wasser gegeben und mit MTBE extrahiert. Die vereinigten organischen Schichten wurden mit Kochsalzlösung gewaschen, über Na2SO4 getrocknet, filtriert und konzentriert, um 3-Amino-5-chlor-6-ethylpyrazin-2-carbonitril zu ergeben.
Schritt 4:
Zu einer Suspension von t-BuONO und CuBr2 in DMF wurde tropfenweise eine Lösung von 3-Amino-5-chlor-6-ethylpyrazin-2-carbonitril in DMF gegeben. Nach Überprüfung durch DC wurde die Reaktionsmischung auf Raumtemperatur abgekühlt und dann in Eis/Wasser gegossen und mit MTBE extrahiert. Die vereinigten organischen Schichten wurden mit Kochsalzlösung gewaschen, über Na2SO4 getrocknet, filtriert und konzentriert, um ein Rohprodukt zu ergeben, das durch Chromatographie gereinigt wurde, um 3-Brom-5-chlor-6-ethylpyrazin-2-carbonitril zu ergeben.
9. Liste der Zwischenprodukte, die wir liefern können
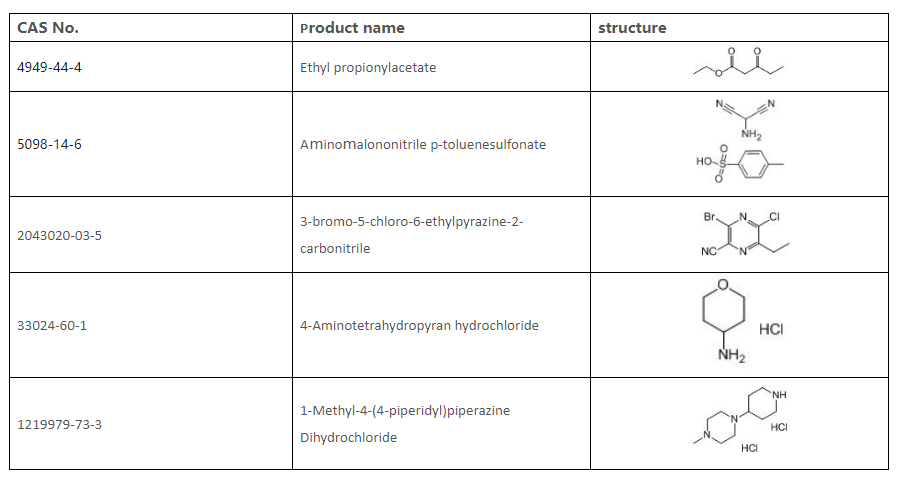
Sandoo Pharmaceutica ist ein professioneller Hersteller von pharmazeutischen Zwischenprodukten. Wir bieten qualitativ hochwertiges Gilteritinib-Fumarat Cas: 1254053-43-4. Herzlich willkommen und wir freuen uns auf Ihre Anfrage!




